LA PRESIÓN DE VAPOR
Es la presión a la que a cada temperatura la fase líquida y vapor se encuentran en equilibrio dinámico; su valor es independiente de las cantidades de líquido y vapor presentes mientras existan ambas. En la situación de equilibrio, las fases reciben la denominación de líquido saturado y vapor saturado. Esta propiedad posee una relación inversamente proporcional con las Fuerzas de Atracción Intermoleculares, debido a que cuanto mayor sea el módulo de las mismas, mayor deberá ser la cantidad de energía entregada (ya sea en forma de calor u otra manifestación) para vencerlas y producir el cambio de estado.
Es la presión a la que a cada temperatura la fase líquida y vapor se encuentran en equilibrio dinámico; su valor es independiente de las cantidades de líquido y vapor presentes mientras existan ambas. En la situación de equilibrio, las fases reciben la denominación de líquido saturado y vapor saturado. Esta propiedad posee una relación inversamente proporcional con las Fuerzas de Atracción Intermoleculares, debido a que cuanto mayor sea el módulo de las mismas, mayor deberá ser la cantidad de energía entregada (ya sea en forma de calor u otra manifestación) para vencerlas y producir el cambio de estado.
La presión de vapor es la presión de un sistema cuando el sólido o liquido se hallan en equilibrio con su vapor.Los vapores y los gases, tienden a ocupar el mayor volumen posible y ejercen así sobre las paredes de los recintos que los contienen, una presión también llamada, fuerza elástica o tensión. Para determinar un valor sobre esta presión se divide la fuerza total por la superficie en contacto.
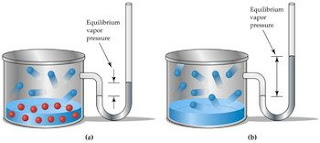
Inicialmente sólo se produce la evaporación ya que no hay vapor; sin embargo a medida que la cantidad de vapor aumenta y por tanto la presión en el interior de la ampolla, se va incrementando también la velocidad de condensación, hasta que transcurrido un cierto tiempo ambas velocidades se igualan. Llegados a este punto se habrá alcanzado la presión máxima posible en la ampolla (presión de vapor o de saturación) que no podrá superarse salvo que se incremente la temperatura.
El equilibrio dinámico se alcanzará más rápidamente cuanta mayor sea la superficie de contacto entre el líquido y el vapor, pues así se favorece la evaporación del líquido; del mismo modo que un charco de agua extenso pero de poca profundidad se seca más rápido que uno más pequeño pero de mayor profundidad que contenga igual cantidad de agua. Sin embargo, el equilibrio se alcanza en ambos casos para igual presión.
El factor más importante que determina el valor de la presión de saturación es la propia naturaleza del líquido, encontrándose que en general entre líquidos de naturaleza similar, la presión de vapor a una temperatura dada es tanto menor cuanto mayor es el peso molecular del líquido.
Inicialmente sólo se produce la evaporación ya que no hay vapor; sin embargo a medida que la cantidad de vapor aumenta y por tanto la presión en el interior de la ampolla, se va incrementando también la velocidad de condensación, hasta que transcurrido un cierto tiempo ambas velocidades se igualan. Llegados a este punto se habrá alcanzado la presión máxima posible en la ampolla (presión de vapor o de saturación) que no podrá superarse salvo que se incremente la temperatura.
El equilibrio dinámico se alcanzará más rápidamente cuanta mayor sea la superficie de contacto entre el líquido y el vapor, pues así se favorece la evaporación del líquido; del mismo modo que un charco de agua extenso pero de poca profundidad se seca más rápido que uno más pequeño pero de mayor profundidad que contenga igual cantidad de agua. Sin embargo, el equilibrio se alcanza en ambos casos para igual presión.
El factor más importante que determina el valor de la presión de saturación es la propia naturaleza del líquido, encontrándose que en general entre líquidos de naturaleza similar, la presión de vapor a una temperatura dada es tanto menor cuanto mayor es el peso molecular del líquido.
PROPIEDADES
La regla de fases establece que la presión del vapor de un líquido puro es función única de la temperatura de saturación. Vemos pues que la presión de vapor en la mayoría de los casos se puede expresar como:
Pvp = f (t)
La cual podría estar relacionada con cualquier otra propiedad intensiva de un líquido saturado ( o vapor), pero es mucho mejor relacionarla directamente con la temperatura de saturación.
¿Cómo se relaciona?
La presión de vapor de un liquido se relaciona con la temperatura por medio de la ecuación de Claussius Clapeyron, sin embargo existen muchas ecuaciones que estudian esta propiedad de los fluidos, pero de todas maneras estas ecuaciones pueden referirse a la ecuación de Clapeyron:
Ln P2/P1 = (DH/R) vaporización (1/T1-1/T2)
Esta ecuación mediante pasos matemáticos, puede convertirse en:
Ln Pvp = A+B/T
ESTIMACION DE VALORES
En intervalos de baja presión: 10 a 1500 mmHg se estima por varios métodos unos de los cuales son:
-.El método de estimación de Frost-Kalkwarf-Thodors, es el mejor para compuestos orgánicos, el cual se hace por medio de Cálculos de tipo iterativo, y arroja un máximo porcentaje de error medio de 5.1%
-.El método de Riedel-Plank-Miller es el mejor para compuestos inorgánicos y además es fácil de usar, este arroja un máximo porcentaje de error medio de 5.2%
-.En intervalos de alta presión: 1500 mmHg hasta la presión critica también existen varios métodos de los cuales mencionare algunos:
-.El método de estimación reducida de Kirchhoff, el cual no es muy exacto pero es muy fácil de usar, este arroja un máximo porcentaje de error medio de 3.2%
-.El método de estimación de Frost-Kalkwarf-Thodors, para intervalos de alta presión también requiere de cálculos iterativos, sin embargo es muy bueno y arroja un máximo porcentaje de error medio de 1.5%
Estos métodos anteriores son métodos trabajados con ecuaciones reducidas para los cuales era necesario conocer tc, pc, tb.. pero existen muchísimos método diferentes tanto con ecuaciones reducidas como con ecuaciones semirreducidas y sin reducir.
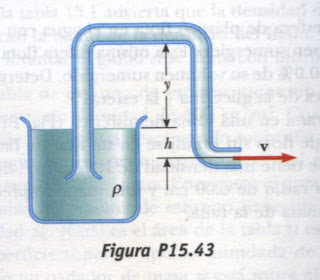
Tipo de uso de la presión de vapor
Para mirar un ejemplo de presión de vapor aplicada a tuberías es bueno analizar un poco las plantas productoras de petroquímicos y refinerías, ya que estas requieren de muchos servicios como: vapor de agua (enfriamiento, servicio, proceso), aire de instrumentos, energía eléctrica; para ello estas plantas necesitan grandes sistemas de transformación de energía, y redes de distribución de varios kilómetros, en las cuales se incurre en perdidas de energía. Para lo que es necesario usar expresiones matemáticas para calcular dichas perdidas y llevar a cabo estudios sobre la recuperación de la inversión y la rentabilidad de acciones de ahorro de energía.
Se debe realizar un pequeño análisis de los sistemas de generación y distribución de vapor, principalmente de aquellos que por ser de gran tamaño son muy dinámicos cambiando sus condiciones de operación; flujo, temperatura y presión varias veces al día. Los cambios pueden ser ocasionados por modificación en las condiciones de operación de las plantas de proceso de mantenimiento predictivo o correctivo de los equipos generadores y consumidores de vapor y energía eléctrica, o por cambio de las condiciones atmosféricas. Estos cambios nos proporcionan áreas de oportunidad de ahorro si se mantiene un análisis constante del sistema de generación y distribución de vapor.
En la generación del vapor vemos como las plantas que lo generan, están formadas por dos o tres niveles de presión, los cuales son distribuidos según su uso o según la magnitud de la presión del vapor, de esta forma: para los bloques de generación eléctrica, turbinas para accionar bombas y compresores de plantas de procesos se usa el vapor de mayor presión; para turbogeneradores eléctricos y grandes turbocompresores, se usa por lo general extracciones de vapor media; las turbinas de menor capacidad normalmente descargan a la red de baja presión.
El control de la presión y la temperatura en las redes de distribución de vapor es sumamente importante, ya que excesos de estas presiones pueden causar un desgaste mas acelerado de la tubería y aparte de esto se pueden generar muchas perdidas de energía, lo cual no es conveniente para un proceso en el cual se esta tratando de aprovechar la energía al máximo.
Para controlar estos excesos o simplemente variantes de las presiones y temperaturas adecuadas se tienen controles de los generadores de vapor los cuales mantienen estos factores en los valores ajustados, esta regulación también se lleva a cabo durante todo el proceso ya que en las redes de media y baja presión, también se cuenta con reguladores de presión y temperatura en turbinas y otros aparatos que intervienen en el este.
Ya con estos reguladores en el procesos, se puede decir que cuando las condiciones de presión y temperatura del vapor que llegan a los equipos varían. La demanda de vapor se ajustará dependiendo de la entalpía y otras características del vapor y del salto entalpico disponible, en el caso de las turbinas.
Para mantener el control en los sistemas de distribución de vapor, es necesario llevar una buena administración y una constante revisión de toda la red, a su ves mediante los dato recolectado durante las revisiones periódicas es necesario estar calculando las perdidas de energía ya que estas afecten directamente la eficiencia del proceso, por ultimo es necesario determinar los puntos de ajuste adecuados para la red.

No hay comentarios:
Publicar un comentario